Уроки хімії мають великий потенціал надихати учнів, особливо коли вони здійснюються у добре оформленому кабінеті. Одним із головних аспектів є вивчення складних неорганічних речовин, які формують основу багатьох хімічних процесів. Давайте розглянемо, як можна організувати інформацію про ці речовини для ефективнішого навчання.
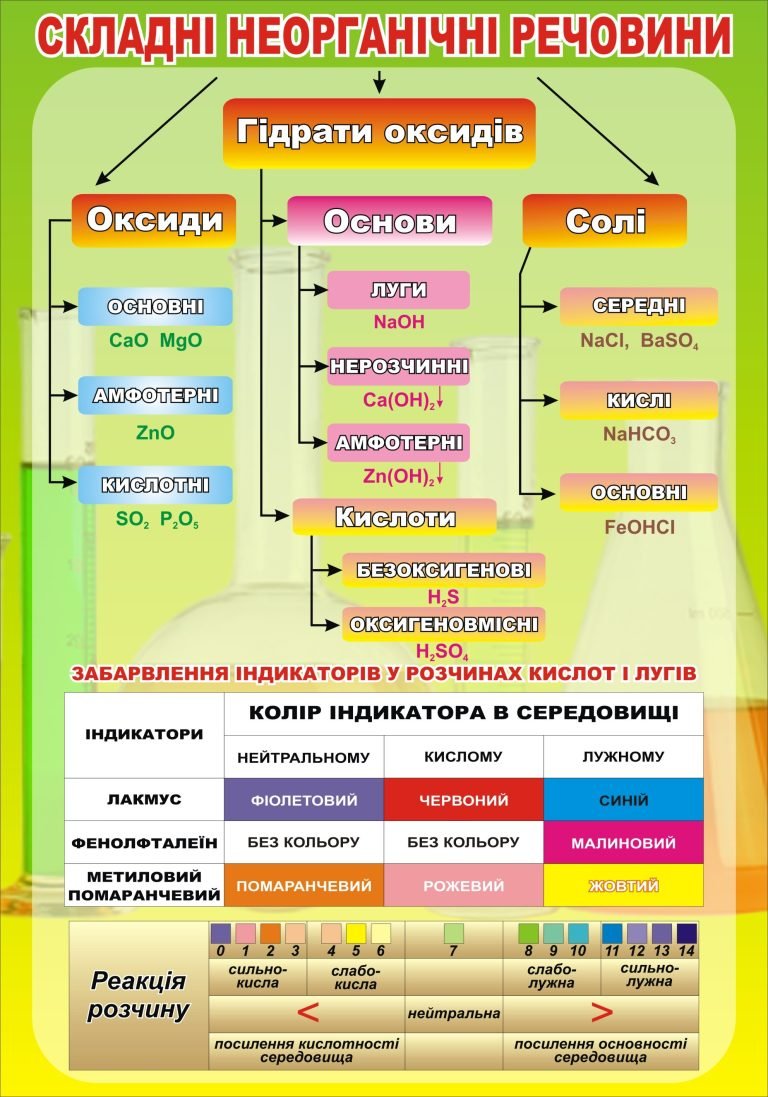
Основні категорії неорганічних речовин
Складні неорганічні речовини класифікуються за кількома категоріями:
- Оксиди
- Основи
- Солі
- Кислоти
Оксиди
Типи оксидів
Оксиди бувають різних типів, зокрема основні, амфотерні та кислотні. Наприклад:
- Основні: CaO, MgO
- Амфотерні: ZnO
- Кислотні: SO2, P2O5
Основи
Різновиди основ
Основи поділяються на луги, нерозчинні і амфотерні:
- Луги: NaOH
- Нерозчинні: Ca(OH)2
- Амфотерні: Zn(OH)2
Кислоти
Види кислот
Кислоти можуть бути безоксигенові та оксигеновмісні:
- Безоксигенові: H2S
- Оксигеновмісні: H2SO4
Солі
Класифікація солей
Солі класифікуються на середні, кислі та основні:
- Середні: NaCl, BaSO4
- Кислі: NaHCO3
- Основні: FeOCl
Індикатори кислотно-лужного середовища
Для визначення кислотності чи лужності середовища використовуються різні індикатори, такі як лакмус, фенолфталеїн і метиловий помаранчевий:
- Лакмус: змінює колір від фіолетового у нейтральному середовищі до червоного у кислотному і синього у лужному.
- Фенолфталеїн: стає малиновим у лужному середовищі.
- Метиловий помаранчевий: змінюється від помаранчевого до жовтого.
Завітайте на сторінку, щоб дізнатися більше про стенд зі складними неорганічними речовинами.